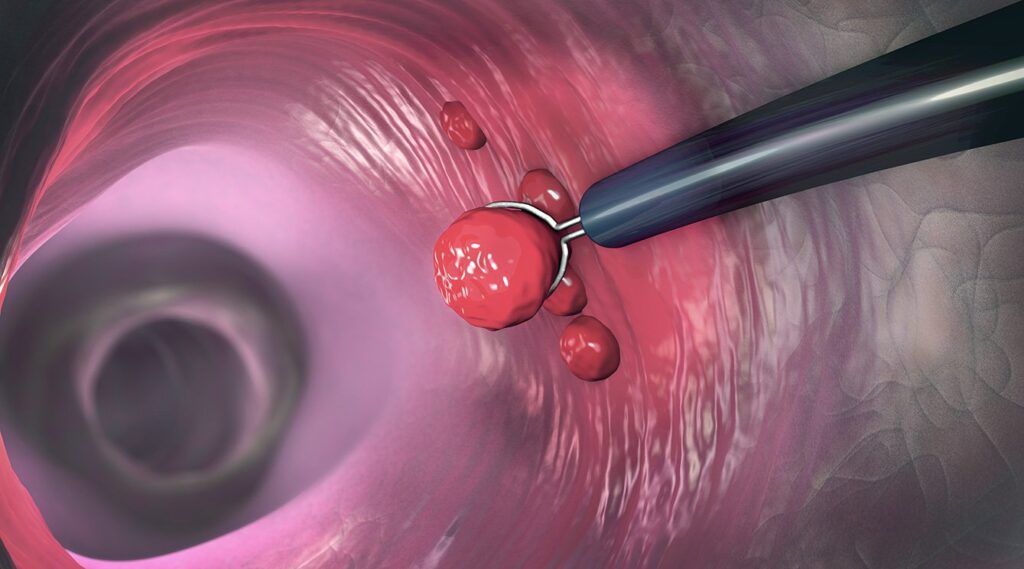
Ο Καρκίνος Παχέος Εντέρου (colon cancer) φαίνεται ότι αναπτύσσεται επί μακρό χρονικό διάστημα. Σήμερα γνωρίζουμε ότι οι περισσότεροι καρκίνοι του παχέος εντέρου ξεκινούν σαν πολύποδες, που είναι γνωστοί και σαν αδενώματα. Με τα χρόνια μπορεί να εξελιχθούν σε καρκίνο.
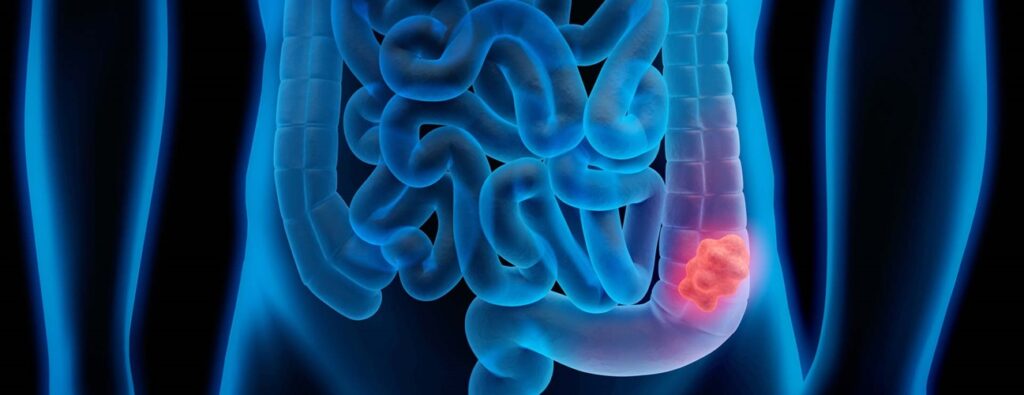
Το παχύ έντερο αποτελείται από 4 τμήματα: το ανιόν, το εγκάρσιο, το κατιόν και το σιγμοειδές. Ο καρκίνος μπορεί να αναπτυχθεί σε οποιοδήποτε από τα 4 τμήματα του εντέρου και μπορεί να έχει διαφορετικά συμπτώματα ανάλογα με τον εντοπισμό του.
Τα κύτταρα από τον όγκο μπορούν να διασπαρούν με την κυκλοφορία του αίματος ή του λεμφικού συστήματος σε άλλα σημεία του σώματος. Εκεί μπορούν να δημιουργήσουν αποικιακούς όγκους, οι οποίοι ονομάζονται μεταστάσεις.
Καρκίνος Εντέρου (colon cancer): Επιδημιολογικά στοιχεία
Ο καρκίνος του παχέος εντέρου είναι ο τρίτος πιο συχνά απαντώμενος καρκίνος σε άνδρες και γυναίκες.
Η θνησιμότητα από καρκίνο του παχέος εντέρου πέφτει διαρκώς τα τελευταία 20 χρόνια. Αυτό μπορεί να οφείλεται στο ότι τα νέα περιστατικά είναι λιγότερα, διαγιγνώσκονται νωρίτερα και οι θεραπείες έχουν βελτιωθεί κατά πολύ.
Η 5ετής επιβίωση είναι 90% για τους ασθενείς που ο καρκίνος τους εντοπίζεται και αντιμετωπίζεται σε αρχικά στάδια, πριν να εξαπλωθεί. Αλλά μόνο περίπου 40% του καρκίνου του παχέος εντέρου εντοπίζονται σε αρχικά στάδια. Γι’ αυτό είναι πολύ σημαντικό να γίνεται έγκαιρη διάγνωση.
Ποιος κινδυνεύει από την ασθένεια;
Ο κίνδυνος εμφάνισης μιας νόσου υπολογίζεται με βάση της ύπαρξη παραγόντων κινδύνου, συνθηκών οι οποίες αποδεδειγμένα αυξάνουν τις πιθανότητες κάποιου να νοσήσει από μια δεδομένη ασθένεια.
Ειδικά για τον καρκίνο του εντέρου υπάρχουν διάφοροι παράγοντες κινδύνου όπως:
Δίαιτα και Διατροφή
- Η θεωρία ότι οι διαιτητικοί παράγοντες σχετίζονται με τον ορθοκολικό καρκίνο βασίζεται σε επιδημιολογικές μελέτες που δείχνουν ότι η θνησιμότητα αυξάνει σε πληθυσμούς που καταναλώνουν πολλές θερμίδες, πολλές πρωτεΐνες ζωικής προέλευσης και κορεσμένα λίπη, και λίγες φυτικές ίνες.
- Οι πληθυσμοί που έχουν αυξημένο ποσοστό στεφανιαίας νόσου και υψηλά επίπεδα χοληστερίνης έχουν και αυξημένο κίνδυνο για εμφάνιση ορθοκολικού καρκίνου. Κάποια είδη λιπών μπορεί να συμβάλλουν κατά το στάδιο ανάπτυξης του καρκίνου.
- Το αλκοόλ είναι ένας ακόμα προδιαθεσικός παράγοντας, χωρίς αυτό να είναι καθολικά παραδεκτό.
- Η αυξημένη πρόσληψη αντιοξειδωτικών συστατικών (όπως βιταμίνη C και Ε) φαίνεται πως μπορεί να μειώσει τον κίνδυνο εμφάνισης αυτού του καρκίνου.
- Η ασπιρίνη φαίνεται ότι παρεμποδίζει την ανάπτυξη όγκων του παχέος εντέρου.
Προσωπικό ιστορικό ορθοκολικού ή άλλου είδους καρκίνου ή πολύποδα
- Οι γυναίκες που έχουν καρκίνο των ωοθηκών, του ενδομητρίου ή του μαστού έχουν μεγαλύτερες πιθανότητες να αναπτύξουν και ορθοκολικό καρκίνο.
- Γενετικοί παράγοντες (οικογενειακό ιστορικό ορθοκολικού καρκίνου ή πολύποδα). Περίπου 25 % των ασθενών έχουν οικογενειακό ιστορικό νόσου.
Ηλικία
Ο κίνδυνος για την εμφάνιση του ορθοκολικού καρκίνου αυξάνει με την ηλικία. Άτομα με ηλικία άνω των 55 ετών έχουν μεγαλύτερο κίνδυνο να αναπτύξουν ορθοκολικό καρκίνο.
Καθιστική ζωή
Η έλλειψη σωματικής άσκησης επηρεάζει την κινητικότητα του εντέρου με αποτέλεσμα να αυξάνει ο κίνδυνος για ορθοκολικό καρκίνο.
Χρόνια Φλεγμονώδης Εντερική Νόσος
Ο ορθοκολικός καρκίνος θεωρείται επιπλοκή χρόνιας φλεγμονώδους εντερικής νόσου και είναι πιο συχνός σε ασθενείς με ελκώδη κολίτιδα. Η επίπτωση της νόσου αυξάνει όσο μεγαλύτερο είναι το τμήμα του εντέρου που έχει προσβληθεί και όσο μεγαλύτερη είναι η διάρκεια και η σοβαρότητα της κολίτιδας.
Συμπτώματα του καρκίνου του Παχέος Εντέρου
Τα συμπτώματα του Καρκίνου Παχέος Εντέρου (colon cancer)μπορεί να είναι ύπουλα ή και απούσα στα αρχικά στάδια. Συνήθως εμφανίζεται αλλαγή στις κενώσεις που επιμένει (συχνότητα, σύσταση, εναλλαγή δυσκοιλιότητας–διάρροιας), αίμα στα κόπρανα (κόκκινο ή σκούρο), πόνος/κράμπες στην κοιλιά, φούσκωμα και αίσθημα ατελούς κένωσης. Συχνά συνυπάρχει ανεξήγητη κόπωση, πτώση βάρους και σιδηροπενική αναιμία (ιδίως σε δεξιό κόλον με «κρυφή» αιμορραγία), ενώ σε αριστερό κόλον είναι πιο συχνή η στένωση των κοπράνων και η βλεννώδης απώλεια. Κάθε νέο ή παρατεινόμενο σύμπτωμα, ειδικά μετά τα 45 ή με οικογενειακό ιστορικό, απαιτεί άμεση αξιολόγηση και συχνά κολονοσκόπηση, καθώς η έγκαιρη διάγνωση αυξάνει θεαματικά τις πιθανότητες πλήρους ίασης.
Διάγνωση καρκίνου παχέος εντέρου
Η διάγνωση του Καρκίνου Παχέος Εντέρου βασίζεται σε συνδυασμό κλινικής εκτίμησης, εργαστηριακών και απεικονιστικών εξετάσεων, με «χρυσό κανόνα» την κολονοσκόπηση. Ξεκινά με λεπτομερές ιστορικό (συμπτώματα, οικογενειακό/γενετικό υπόβαθρο, φλεγμονώδεις νόσοι εντέρου, πολυποδιάσεις) και κλινική εξέταση· ακολουθεί γενική αίματος (αναζήτηση σιδηροπενικής αναιμίας), σίδηρος/φερριτίνη και CEA ως baseline δείκτης. Για τον προσυμπτωματικό έλεγχο χρησιμοποιείται ετησίως FIT (ή FOBT), όμως κάθε θετικό τεστ πρέπει να επιβεβαιώνεται με πλήρη κολονοσκόπηση, η οποία επιτρέπει εντόπιση της βλάβης, βιοψίες για ιστολογική διάγνωση και, όπου ενδείκνυται, πολυποδεκτομή. Στην κολονοσκόπηση φροντίζουμε για πλήρη επισκόπηση έως τον τυφλό και tattoo/clip για ακριβή προεγχειρητικό εντοπισμό. Αν υπάρχει απόφραξη ή ατελής εξέταση, μπορεί να χρησιμοποιηθεί CT κολονογραφία ή επανάληψη κολονοσκόπησης μετά την αποσυμφόρηση/επέμβαση. Μετά την ιστολογική επιβεβαίωση, γίνεται σταδιοποίηση με CT θώρακος–κοιλίας–πυέλου με σκιαγραφικό (± MRI ήπατος για ύποπτες εστίες) και καταγραφή κατά TNM· για χαμηλές βλάβες ορθού απαιτείται MRI πυέλου υψηλής ευκρίνειας (και, σε επιλεγμένες περιπτώσεις, EUS) για εκτίμηση τοιχωματικής διήθησης/μεσοορθικού φάσματος. Παράλληλα διενεργείται μοριακός χαρακτηρισμός (MMR/MSI, KRAS/NRAS/BRAF) που κατευθύνει συστηματικές θεραπείες. Η τελική θεραπευτική στρατηγική καθορίζεται σε διεπιστημονικό ογκολογικό συμβούλιο (MDT), συνδυάζοντας ευρήματα, χειρουργησιμότητα και τη γενική κατάσταση του ασθενούς.
Διαγνωστική Διαδικασία:
- Ιστορικό & εξέταση: συμπτώματα, ηλικία/οικογενειακό ιστορικό, γενική κλινική αξιολόγηση.
- Εξετάσεις αίματος: γενική αίματος (αναιμία), σίδηρος/φερριτίνη, CEA ως αρχική τιμή.
- Προσυμπτωματικός έλεγχος: ετήσιο FIT (ή FOBT). Αν βγει θετικό → κολονοσκόπηση.
- Κολονοσκόπηση (gold standard): εντοπισμός βλάβης, βιοψίες για ιστολογική διάγνωση, αφαίρεση πολύποδων όπου είναι εφικτό.
- Πληρότητα εξέτασης: έλεγχος μέχρι τον τυφλό, καλή προετοιμασία, τοποθέτηση tattoo/clip για ακριβή προεγχειρητικό εντοπισμό.
- Εναλλακτικές/συμπληρωματικές: CT κολονογραφία αν η κολονοσκόπηση δεν μπορεί να ολοκληρωθεί (π.χ. απόφραξη).
- Σταδιοποίηση μετά τη διάγνωση: αξονική τομογραφία θώρακος–κοιλίας–πυέλου με σκιαγραφικό (± MRI ήπατος για ύποπτες εστίες).
- Καρκίνος ορθού: επιπλέον MRI πυέλου υψηλής ευκρίνειας (± ενδοορθικός υπέρηχος).
- Μοριακός έλεγχος: MMR/MSI, KRAS/NRAS/BRAF για καθοδήγηση της συστηματικής θεραπείας.
- Απόφαση θεραπείας: συζήτηση σε ογκολογικό συμβούλιο (MDT) με βάση όλα τα παραπάνω και τη γενική κατάσταση του ασθενούς.
Ο μοριακός έλεγχος είναι σαν «ταυτότητα» του όγκου: από το δείγμα βιοψίας/επέμβασης εξετάζουμε συγκεκριμένα γονίδια/δείκτες για να δούμε ποια φάρμακα ταιριάζουν καλύτερα. Αν ο όγκος είναι MSI-H/dMMR, συνήθως ανταποκρίνεται καλά στην ανοσοθεραπεία. Αν έχει αλλαγές στα RAS (KRAS/NRAS), τότε δεν ωφελείται από κάποια στοχευμένα φάρμακα (anti-EGFR). Η μετάλλαξη BRAF V600E δείχνει πιο «επιθετικό» τύπο και κατευθύνει σε ειδικούς συνδυασμούς φαρμάκων. Μερικές φορές βρίσκουμε HER2 ή NTRK, που ανοίγουν δρόμο για στοχευμένες θεραπείες ακριβείας. Σημαντικό: αυτός ο έλεγχος αφορά τον όγκο, όχι εσάς ως άτομο (δεν είναι «τεστ κληρονομικότητας») και μας βοηθά να προσωποποιήσουμε τη θεραπεία.
Ο προσυμπτωματικός έλεγχος (screening) είναι ο πιο απλός τρόπος να προλάβουμε τον καρκίνο παχέος εντέρου πριν καν εμφανιστούν συμπτώματα. Σε άτομα μέσου κινδύνου ο έλεγχος ξεκινά περίπου στα 45 έτη (σε πολλές ευρωπαϊκές χώρες 50–74/75). Πρακτικά, έχετε δύο βασικές επιλογές: ετήσιο τεστ κοπράνων (FIT) και, αν βγει θετικό, κολονοσκόπηση, ή κολονοσκόπηση προληπτικά κάθε 5 χρόνια. Η κολονοσκόπηση μπορεί να αφαιρέσει πολύποδες πριν εξελιχθούν σε καρκίνο—γι’ αυτό σώζει ζωές. Όσοι έχουν οικογενειακό ιστορικό ή άλλους παράγοντες κινδύνου ξεκινούν νωρίτερα και πιο συχνά, με οδηγίες εξατομίκευσης από τον γιατρό. Στην πρόληψη βοηθούν επίσης η μεσογειακή διατροφή, η διατήρηση υγιούς βάρους, η άσκηση, και η αποφυγή καπνίσματος/περίσσειας αλκοόλ. Αν έχετε απορίες για το ποιο σχήμα ταιριάζει σε εσάς, μιλήστε με τον γιατρό σας—η σωστή επιλογή είναι αυτή που θα κάνετε με συνέπεια.
Καρκίνος Παχέος Εντέρου (colon cancer) – Θεραπεία
Συνήθως υπάρχουν πολλές εναλλακτικές θεραπείες.
Υπάρχου τρεις βασικοί τύποι θεραπείας του καρκίνου του παχέος εντέρου:
- εγχείρηση
- ακτινοβολία
- χημειοθεραπεία
Ανάλογα με το στάδιο του καρκίνου, μπορεί να χορηγηθούν δύο ή και τρεις τύποι θεραπείας ταυτόχρονα ή διαδοχικά.
Χειρουργική Θεραπεία Του Καρκίνου Του Παχέος Εντέρου
Στόχοι επέμβασης και ογκολογικές αρχές
Στόχος είναι εκτομή R0, επαρκής λεμφαδενικός καθαρισμός (≥12 λεμφαδένες) και ατραυματική εκτομή κατά τις εμβρυολογικές στιβάδες. Όπου ενδείκνυται, εφαρμόζεται Complete Mesocolic Excision (CME) με κεντρική αγγειακή απολίνωση (CVL), που συνδυάζει ογκολογικά καθαρά όρια με εκτεταμένη λεμφαδενεκτομή. Η παθολογοανατομική σταδιοποίηση γίνεται κατά TNM, και το τελικό πλάνο εναρμονίζεται με διεθνείς οδηγίες (NCCN/ESMO).
Η εκτομή R0 σημαίνει ότι ο όγκος έχει αφαιρεθεί ολόκληρος και τα χειρουργικά όρια (margins) είναι αρνητικά στο μικροσκόπιο—δηλαδή δεν υπάρχει υπολειπόμενος καρκινικός ιστός στα άκρα του παρασκευάσματος.
- R0: καθαρά (αρνητικά) μικροσκοπικά όρια → καλύτερη πρόγνωση.
- R1: μικροσκοπικά θετικά όρια (μικροσκοπικό υπόλειμμα όγκου).
- R2: μακροσκοπικό υπόλειμμα όγκου (φαίνεται με γυμνό μάτι/απεικόνιση).
Στον καρκίνο παχέος/ορθού, η επιδίωξη είναι πάντα R0, κάτι που επιβεβαιώνεται από τον παθολογοανατόμο στην έκθεση. Ιδιαίτερη σημασία έχει και το περιφερικό/κυκλοτερώς όριο (CRM) στο ορθό: αν είναι ελεύθερο, μειώνεται ο κίνδυνος υποτροπής.
Προσπέλαση: Ανοικτή – Λαπαροσκοπική – Ρομποτική
Η επιλογή προσπέλασης εξατομικεύεται βάσει ανατομίας, συννοσηροτήτων, BMI, εμπειρίας κέντρου και εντόπισης όγκου. Η λαπαροσκοπική και η ρομποτική κολεκτομή προσφέρουν ισοδύναμα ογκολογικά αποτελέσματα σε κατάλληλα επιλεγμένους ασθενείς, με τυπικά λιγότερο πόνο και ταχύτερη ανάρρωση σε σχέση με την ανοικτή. Η ρομποτική μπορεί να διευκολύνει σε τεχνικά απαιτητικές πυελικές εκτομές (στενή λεκάνη, παχυσαρκία), πάντα στο πλαίσιο εμπειρίας ομάδας και πρωτοκόλλων ποιότητας.
Ασφάλεια αναστόμωσης και ICG-φθορισμογραφία
Η ορθή τεχνική, ο καλός αγγειακός εφοδιασμός και η χαμηλή τάση της αναστόμωσης είναι κρίσιμα για τη μείωση διαφυγής. Η ICG-φθορισμογραφία μπορεί να βοηθήσει στην εκτίμηση αιμάτωσης πριν το ράψιμο· μετα-αναλύσεις υποδεικνύουν πιθανό όφελος στη μείωση διαφυγών, αν και τα δεδομένα δεν είναι απολύτως ομοιογενή και απαιτούνται περαιτέρω RCTs. Χρησιμοποιείται ως συμπληρωματικό εργαλείο, όχι ως υποκατάστατο της χειρουργικής κρίσης.
ERAS και μετεγχειρητική πορεία
Η εφαρμογή ERAS (πρώιμη σίτιση/κινητοποίηση, στοχευμένη αναλγησία, περιορισμός σωλήνων/οπιοειδών) βελτιώνει την ανάρρωση και μειώνει επιπλοκές και διάρκεια νοσηλείας. Επίκαιρες οδηγίες περιγράφουν αναλυτικά τα προ-, διεγχειρητικά και μετεγχειρητικά στοιχεία που πρέπει να τηρούνται συστηματικά από την ομάδα.
Ειδικά σενάρια: Απόφραξη παχέος εντέρου
Σε αποφρακτικό καρκίνο (κυρίως αριστερού κόλου), η τοποθέτηση ενδοσκοπικού stent (SEMS) ως bridge-to-surgery είναι αποδεκτή επιλογή σε επιλεγμένους ασθενείς/κέντρα, στο πλαίσιο ενημερωμένης συναπόφασης (διαθέσιμη τεχνογνωσία, κίνδυνος διάτρησης/υποτροπής vs χαμηλότερες άμεσες επιπλοκές και λιγότερες μόνιμες στομίες). Για καθαρά παρηγορική αντιμετώπιση της απόφραξης, τα stents αποτελούν συνήθως προτιμώμενη λύση.
Όγκοι ορθού (εφόσον σχετίζεται με το τρέχον case)
Για μέσο/κάτω ορθό, πρότυπο είναι η Total Mesorectal Excision (TME) (ή TaTME σε επιλεγμένα κέντρα). Σε χαμηλές αναστομώσεις συχνά τίθεται προστατευτική ειλεοστομία. Σε πλήρη κλινική ανταπόκριση μετά συνολική νεοεπικουρική θεραπεία (TNT), η στρατηγική watch-and-wait εφαρμόζεται σε εξειδικευμένα κέντρα με αυστηρό follow-up (ενδοσκόπηση/DRE/MRI ανά 3 μήνες τα πρώτα 2 έτη).
Τι καθορίζει το τελικό πλάνο
Το θεραπευτικό πλάνο οριστικοποιείται σε διεπιστημονικό ογκολογικό συμβούλιο (MDT), συνδυάζοντας TNM στάδιο, μοριακό προφίλ (MMR/MSI, RAS/BRAF, κ.ά.), χειρουργησιμότητα/συννοσηρότητες και προτιμήσεις ασθενούς, σύμφωνα με αλγόριθμους NCCN/ESMO.
Τα συρραπτικά εργαλεία: Αυτά αποτελούν τα πλέον σύγχρονα αυτόματα μηχανήματα, με τα οποία ο γενικός χειρουργός επιτελεί: γρήγορες κινήσεις διατομής εκτομής και αναστόμωσης του εντέρου, με παράλληλη ιδανική ασηψία και ανατομική αρτιότητα.
Λαπαροσκοπική Χειρουργική
Η λαπαροσκοπική κολεκτομή είναι ελάχιστα επεμβατική τεχνική με ισοδύναμα ογκολογικά αποτελέσματα σε σύγκριση με την ανοικτή χειρουργική, όταν εφαρμόζεται από έμπειρες ομάδες και σε κατάλληλα επιλεγμένους ασθενείς. Τα οφέλη περιλαμβάνουν λιγότερο μετεγχειρητικό πόνο, ταχύτερη ανάρρωση και βραχύτερη νοσηλεία, με διατήρηση καθαρών ορίων εκτομής και επαρκούς λεμφαδενεκτομής (≥12 λεμφαδένες). Η επιλογή προσπέλασης εξατομικεύεται (BMI, συμφύσεις/ιστορικό, εντόπιση όγκου, εμπειρία κέντρου) και εντάσσεται σε πρωτόκολλα ERAS για καλύτερη ανάρρωση. Σε επιλεγμένες περιπτώσεις χρησιμοποιείται ICG-φθορισμογραφία για έλεγχο αιμάτωσης της αναστόμωσης. Σε σπάνιες περιπτώσεις μπορεί να απαιτηθεί μετατροπή σε ανοικτή, για λόγους ασφάλειας.
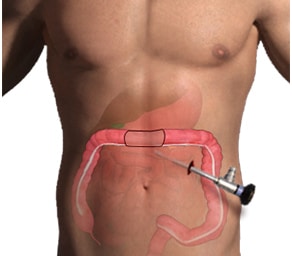
Επίσης προσφέρει μία αρτιότερη και πλέον αναίμακτη επέμβαση σε δύσκολα προσβάσιμες περιοχές της κοιλιάς όπως η “σπληνική καμπή” και η ελάσσων πύελος, με αποτέλεσμα την μείωση της σημαντικής νοσηρότητας αυτών των επεμβάσεων.
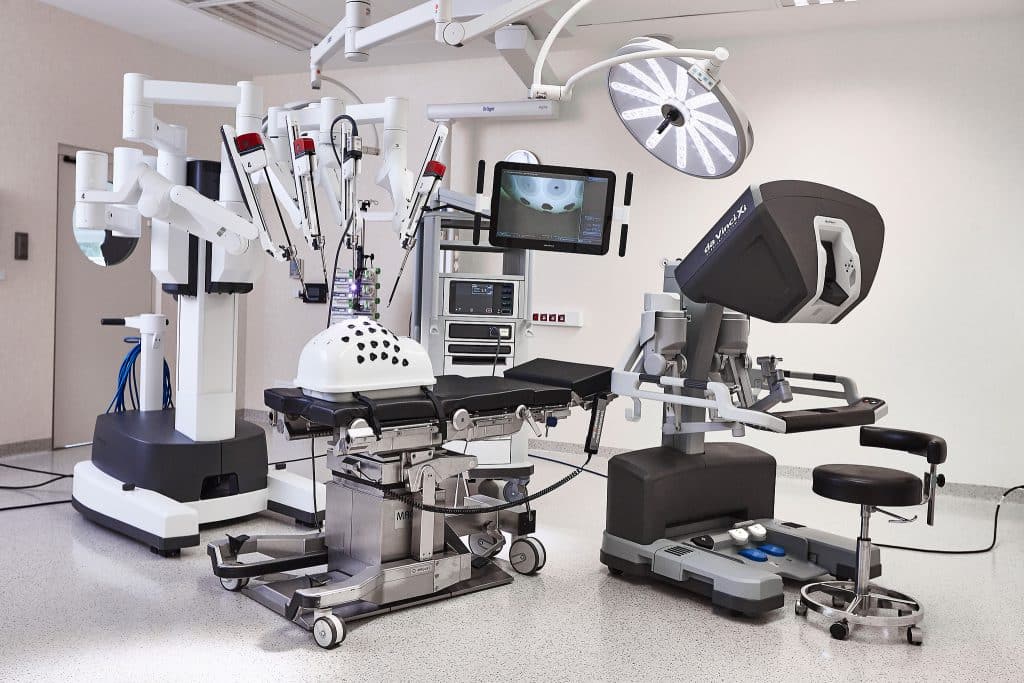
Ρομποτική Κολεκτομή
Η ρομποτική κολεκτομή είναι ελάχιστα επεμβατική επέμβαση που αξιοποιεί 3D υψηλής ευκρίνειας όραση και αρθρωτά εργαλεία για ακριβή παρασκευή αγγείων και μεσοκόλου, ιδίως σε τεχνικά απαιτητικές περιοχές (σπληνική καμπή, παχύσαρκοι ασθενείς, συμφύσεις/επανεπεμβάσεις). Σε κατάλληλα επιλεγμένους ασθενείς και σε έμπειρα κέντρα, προσφέρει ισοδύναμα ογκολογικά αποτελέσματα με την ανοικτή/λαπαροσκοπική (καθαρά όρια, επαρκείς λεμφαδένες), με δυνατότητα χαμηλότερων μετατροπών σε ανοικτή και σταθερά εργονομία για τον χειρουργό. Συχνά συνδυάζεται με ERAS (νωρίς σίτιση/κινητοποίηση), ενώ μπορεί να χρησιμοποιηθεί ICG-φθορισμογραφία για έλεγχο αιμάτωσης της αναστόμωσης και, όπου ενδείκνυται (π.χ. δεξιά κολεκτομή), ενδοκοιλιακή αναστόμωση που διευκολύνει την ανάρρωση. Η επιλογή πλατφόρμας παραμένει εξατομικευμένη—με γνώμονα το στάδιο, τα χαρακτηριστικά του ασθενούς και, κυρίως, την εμπειρία της ομάδας και την ασφάλεια.
Ακτινοβολία – Πότε χρειάζεται.
Η ακτινοθεραπεία χρειάζεται κυρίως στους όγκους του ορθού. Τη δίνουμε πριν από το χειρουργείο για να μικρύνει ο όγκος και να αυξηθούν οι πιθανότητες πλήρους, ασφαλούς αφαίρεσης—ειδικά όταν φαίνεται «προχωρημένος» στην MRI (βάθος διήθησης, λεμφαδένες, πολύ κοντά σε ζωτικά ανατομικά όρια). Μερικές φορές μπορεί να χρειαστεί μετά το χειρουργείο αν τα όρια δεν ήταν απόλυτα καθαρά. Στον καρκίνο του κόλου (εκτός ορθού) σπάνια χρησιμοποιείται· συνήθως μόνο παρηγορικά για πόνο ή αιμορραγία, ή σε ιδιαίτερες περιπτώσεις όταν δεν μπορεί να γίνει ξανά επέμβαση. Για μεμονωμένες μεταστάσεις (π.χ. σε ήπαρ/πνεύμονα) που δεν αφαιρούνται χειρουργικά, μπορεί να εφαρμοστεί στοχευμένη ακτινοβολία υψηλής ακρίβειας (SBRT). Η απόφαση λαμβάνεται σε ογκολογικό συμβούλιο (MDT) και προσαρμόζεται στο δικό σας ιστορικό, με στόχο το καλύτερο αποτέλεσμα με τη μικρότερη δυνατή επιβάρυνση.
Χημειοθεραπεία Ενδείξεις.
Η χημειοθεραπεία είναι φάρμακα που κυκλοφορούν στο αίμα και σκοτώνουν μικροσκοπικά καρκινικά κύτταρα. Ο στόχος της αλλάζει ανάλογα με το στάδιο:
- Μετά το χειρουργείο (κόλον):
- Στάδιο ΙΙ με “υψηλό ρίσκο” ή Στάδιο ΙΙΙ → δίνουμε χημειοθεραπεία για να μειώσουμε τις πιθανότητες υποτροπής.
- Συνήθως κρατά 3–6 μήνες (συνδυασμοί τύπου CAPOX/FOLFOX).
- Πριν/μετά το χειρουργείο (ορθό):
- Σε πιο προχωρημένους όγκους ορθού, δίνουμε πριν την επέμβαση (συχνά μαζί με ακτινοβολία) για να μικρύνει ο όγκος και να γίνει πιο ασφαλής/ριζική η αφαίρεση. Μερικές φορές συνεχίζεται και μετά, ανάλογα με τα ευρήματα.
- Σε μεταστάσεις:
- Χρησιμοποιείται για έλεγχο της νόσου, συρρίκνωση μεταστάσεων και —όταν γίνεται— για να καταστήσει εφικτή την αφαίρεσή τους (π.χ. στο ήπαρ).
- Προσθέτουμε στοχευμένα φάρμακα ανάλογα με τα μοριακά χαρακτηριστικά του όγκου.
- Αν ο όγκος έχει ειδικά χαρακτηριστικά (MSI-H/dMMR), μπορεί να προτιμηθεί ανοσοθεραπεία αντί για κλασική χημειοθεραπεία.
Τι να περιμένετε: η αγωγή δίνεται σε κύκλους (ανά 2–3 εβδομάδες ή καθημερινά χάπια με διαλείμματα), με συχνή παρακολούθηση αίματος. Πιθανές ανεπιθύμητες ενέργειες (κούραση, ναυτία, διάρροια, μουδιάσματα στα άκρα) ελέγχονται με υποστηρικτικά φάρμακα και προσαρμογές δόσης.
Ποιος αποφασίζει; Η επιλογή γίνεται εξατομικευμένα στο ογκολογικό συμβούλιο (MDT), με βάση το στάδιο, τη γενική σας κατάσταση και το μοριακό προφίλ του όγκου. Στόχος μας είναι το μέγιστο όφελος με τη μικρότερη δυνατή επιβάρυνση.
Συστάσεις για τη διατροφή
Οι συστάσεις που δίδονται από την Παγκόσμια Οργάνωση Υγείας σε συνεργασία με έγκυρα διεθνή αντικαρκινικά κέντρα όσον αφορά την δίαιτα και τον τρόπο ζωής στην πρόληψη του Κ.Π.Ε. είναι:
- Μειωμένη κατανάλωση ζωικού λίπους (λιγότερο από το 20% του συνόλου των λαμβανομένων θερμίδων).
- Η καθημερινή διατροφή να περιλαμβάνει ικανή ποσότητα φρέσκων λαχανικών και φρούτων, ψωμιού ολικής αλέσεως, δημητριακών, οσπρίων και ελαιολάδου, προκειμένου να εξασφαλισθεί η λήψη σημαντικής ποσότητας φυτικών ινών, βιταμινών, ιχνοστοιχείων και άλλων συστατικών που έχουν αντικαρκινική δράση. Υπάρχουν ενδείξεις ότι το ασβέστιο των γαλακτοκομικών προϊόντων ασκεί προφυλακτική δράση. Το παραπάνω διαιτολόγιο αντιπροσωπεύεται στη λεγόμενη «Μεσογειακή Δίαιτα».
Το παραπάνω προτεινόμενο διαιτολόγιο και ο δραστικός περιορισμός του Δυτικού τρόπου διατροφής με τροφές του τύπου «Fast Fοοd», που είναι πολύ υψηλής περιεκτικότητας σε λίπος, είναι πιθανώς ευεργετικό, όταν εφαρμόζεται από την παιδική και νεαρή ηλικία.
Να αποφεύγονται:
- Η υπερβολική λήψη θερμίδων και η παχυσαρκία
- Το κάπνισμα ή κατάχρηση οινοπνευματωδών
- Η σωματική άσκηση πρέπει να είναι καθημερινή πρακτική
Συμπερασματικά, είναι χρήσιμη η διατροφή που είναι φτωχή σε ζωικό λίπος και πλούσια σε συστατικά φυτικής προέλευσης, αλλά μέχρι να διευκρινισθούν με ακρίβεια οι ιδιότητες των διαφόρων συστατικών της τροφής, πρέπει να αποφεύγονται οι διαιτητικές υπερβολές.
Συχνές ειδικές ερωτήσεις για τον καρκίνο παχέος εντέρου
Αν έχετε διαγνωστεί με καρκίνο παχέος εντέρου ή βρίσκεστε σε διαδικασία ελέγχου, οι παρακάτω ενότητες βοηθούν να κατανοήσετε καλύτερα τη διάγνωση, τη χειρουργική θεραπεία, την ανάρρωση και την παρακολούθηση μετά την επέμβαση.
Σημείωση: Οι παραπάνω πληροφορίες λειτουργούν συμπληρωματικά. Η τελική θεραπευτική απόφαση για τον καρκίνο παχέος εντέρου βασίζεται στη θέση του όγκου, το στάδιο, τη γενική κατάσταση του ασθενούς και την εκτίμηση της χειρουργικής και ογκολογικής ομάδας.
FAQ – Συχνές Ερωτήσεις
- Ποια συμπτώματα να με ανησυχήσουν για καρκίνο παχέος εντέρου;
- Αλλαγές στις κενώσεις (διάρροια/δυσκοιλιότητα) που επιμένουν, αίμα στα κόπρανα ή μαύρα κόπρανα, ανεξήγητη αναιμία/κόπωση, απώλεια βάρους, επίμονος κοιλιακός πόνος και αίσθημα ατελούς κένωσης. Σε έντονο πόνο με φούσκωμα/εμέτους (υποψία απόφραξης) ζητήστε άμεσα ιατρική βοήθεια.
- Πότε χρειάζεται προληπτικός έλεγχος (screening) και ποια εξέταση προτιμάται;
- Σε άτομα μέσου κινδύνου, ο προληπτικός έλεγχος ξεκινά συνήθως γύρω στα 45. Η κολονοσκόπηση είναι η εξέταση αναφοράς. Εναλλακτικά μπορούν να γίνουν μη επεμβατικές δοκιμασίες κοπράνων, αλλά θετικό αποτέλεσμα χρειάζεται κολονοσκόπηση. Σε αυξημένο κίνδυνο (οικογενειακό ιστορικό, ΙΦΝΕ, κληρονομικά σύνδρομα) ο έλεγχος αρχίζει νωρίτερα και εξατομικεύεται.
- Πώς γίνεται η διάγνωση και η σταδιοποίηση;
- Η διάγνωση τίθεται με κολονοσκόπηση και βιοψίες. Η σταδιοποίηση περιλαμβάνει απεικόνιση (συνήθως αξονική θώρακος–κοιλίας–πυέλου) και εργαστηριακούς δείκτες όπως CEA, ώστε να σχεδιαστεί σωστά η θεραπεία.
- Ποιες είναι οι χειρουργικές επιλογές και τι να περιμένω με ERAS;
- Η ογκολογικά ορθή κολεκτομή μπορεί να γίνει ανοικτά, λαπαροσκοπικά ή ρομποτικά. Τα ελάχιστα επεμβατικά (λαπαροσκόπηση/ρομποτική) συνδέονται με λιγότερο πόνο και ταχύτερη ανάρρωση. Με ERAS στοχεύουμε σε γρήγορη κινητοποίηση, πρώιμη σίτιση και συνήθως μικρότερη νοσηλεία, πάντα ανάλογα με το στάδιο και τη γενική κατάσταση.
- Πώς γίνεται η παρακολούθηση μετά τη θεραπεία;
- Υπάρχει οργανωμένο follow-up για 5 χρόνια περίπου: τακτική κλινική εκτίμηση, CEA όπου ενδείκνυται, προγραμματισμένες απεικονίσεις και κολονοσκόπηση (συνήθως στον 1ο χρόνο και κατόπιν ανά 3–5 χρόνια, ανάλογα με τα ευρήματα).
Τελευταία ιατρική επιμέλεια: 22/04/2026 από τον Δρ. Γεώργιος Σάμπαλης, MD, PhD

