Η λέξη «ανοσοθεραπεία» ακούγεται ολοένα και πιο συχνά στην ογκολογία — και όχι άδικα. Πρόκειται για θεραπείες που δεν “χτυπούν” άμεσα το καρκινικό κύτταρο όπως η κλασική χημειοθεραπεία, αλλά ενισχύουν ή “ξεκλειδώνουν” την ικανότητα του ανοσοποιητικού να αναγνωρίζει και να καταστρέφει τον όγκο. Αυτό, όμως, δεν σημαίνει ότι ταιριάζει σε όλους ή ότι λειτουργεί πάντα με τον ίδιο τρόπο. Ανοσοθεραπεία στην κακοήθεια: τι είναι και πού εφαρμόζεται.

Τι είναι η ανοσοθεραπεία (με απλά λόγια)
Το ανοσοποιητικό μας σύστημα έχει μηχανισμούς επιτήρησης που εντοπίζουν “ξένα” ή ανώμαλα κύτταρα. Οι καρκίνοι, όμως, συχνά:
- κρύβονται από το ανοσοποιητικό,
- το “φρενάρουν” μέσω ειδικών μορίων,
- ή δημιουργούν ένα μικροπεριβάλλον που μπλοκάρει την άμυνα.
Η ανοσοθεραπεία στοχεύει να αντιστρέψει αυτά τα “κόλπα” του όγκου.
Κύριες κατηγορίες ανοσοθεραπείας
1) Αναστολείς “immune checkpoints” (anti-PD-1, anti-PD-L1, anti-CTLA-4)
Είναι η πιο γνωστή μορφή ανοσοθεραπείας. Τα “checkpoints” λειτουργούν σαν φρένα για να μην υπερενεργοποιείται η άμυνα. Κάποιοι όγκοι τα εκμεταλλεύονται για να μην τους επιτίθεται το ανοσοποιητικό.
Με τους αναστολείς checkpoints, αφαιρείται το φρένο και τα Τ-λεμφοκύτταρα μπορούν να δράσουν πιο αποτελεσματικά.
Πού χρησιμοποιούνται συχνά (ενδεικτικά):
- μελάνωμα
- μη μικροκυτταρικός καρκίνος πνεύμονα (NSCLC)
- καρκίνος νεφρού
- ουροθηλιακός καρκίνος (ουροδόχος κύστη)
- καρκίνος κεφαλής-τραχήλου
- ορισμένοι γαστρεντερικοί καρκίνοι, ειδικά όταν υπάρχουν συγκεκριμένοι βιοδείκτες (π.χ. MSI-H/dMMR)
2) Μονοκλωνικά αντισώματα (και “ανοσολογικά” αντισώματα)
Ορισμένα αντισώματα:
- βοηθούν το ανοσοποιητικό να αναγνωρίσει καλύτερα τον όγκο,
- ή “κουβαλούν” πάνω τους φάρμακο/ραδιοϊσότοπο (antibody-drug conjugates – αυτά είναι συγγενικά αλλά όχι πάντα καθαρή ανοσοθεραπεία με τη στενή έννοια).
3) Κυτταρικές θεραπείες (π.χ. CAR-T)
Εδώ “εκπαιδεύονται” κύτταρα του ίδιου του ασθενή (συνήθως Τ-κύτταρα) ώστε να αναγνωρίζουν συγκεκριμένο στόχο σε καρκινικά κύτταρα.
Κυρίως εφαρμογές σήμερα:
- αιματολογικές κακοήθειες (ορισμένα λεμφώματα, ορισμένες λευχαιμίες, πολλαπλούν μυέλωμα σε επιλεγμένες ενδείξεις)
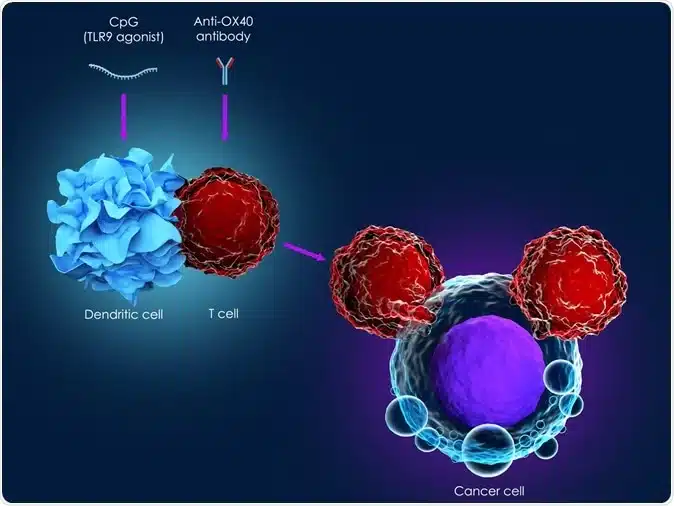
4) Διειδικά αντισώματα (bispecific antibodies)
Λειτουργούν σαν “γέφυρα” που φέρνει σε επαφή Τ-κύτταρα με καρκινικά κύτταρα, ενισχύοντας τη στοχευμένη ανοσολογική επίθεση. Χρησιμοποιούνται κυρίως σε αιματολογικές κακοήθειες και αναπτύσσονται και για συμπαγείς όγκους.
5) Θεραπευτικά εμβόλια, κυτταροκίνες, ογκο-ιοί (oncolytic viruses)
- Τα θεραπευτικά εμβόλια δεν είναι σαν τα εμβόλια πρόληψης. Στόχος τους είναι να εκπαιδεύσουν την άμυνα απέναντι σε αντιγόνα του όγκου.
- Οι κυτταροκίνες (π.χ. ιντερλευκίνες) έχουν πιο ειδικές και περιορισμένες ενδείξεις λόγω τοξικότητας.
- Οι ογκο-ιοί μολύνουν επιλεκτικά καρκινικά κύτταρα και ενεργοποιούν ανοσολογική απάντηση (σε συγκεκριμένες περιπτώσεις).
Πού εφαρμόζεται στην πράξη: “πότε έχει νόημα;”
Η ανοσοθεραπεία μπορεί να δοθεί:
- ως πρώτη γραμμή (μόνη της ή σε συνδυασμό, π.χ. με χημειοθεραπεία),
- ως δεύτερη/τρίτη γραμμή όταν έχουν προηγηθεί άλλες θεραπείες,
- επικουρικά (adjuvant) μετά από χειρουργείο για μείωση κινδύνου υποτροπής,
- νεοεπικουρικά (neoadjuvant) πριν από χειρουργείο για συρρίκνωση/έλεγχο νόσου σε επιλεγμένα πρωτόκολλα,
- σε μεταστατική νόσο για έλεγχο και παράταση επιβίωσης σε κατάλληλους ασθενείς.
Συχνά, το “κλειδί” είναι η σωστή επιλογή ασθενών.
Βιοδείκτες που επηρεάζουν την επιλογή (πολύ σημαντικό)
Δεν είναι όλες οι κακοήθειες το ίδιο “ορατές” στο ανοσοποιητικό. Γι’ αυτό, σε αρκετούς όγκους αξιολογούνται δείκτες όπως:
- PD-L1 έκφραση (όχι απόλυτος κανόνας, αλλά χρήσιμος οδηγός σε ορισμένες ενδείξεις)
- MSI-H / dMMR (υψηλή μικροδορυφορική αστάθεια/έλλειμμα επιδιόρθωσης DNA) — συνδέεται με καλύτερη πιθανότητα ανταπόκρισης σε ορισμένες περιπτώσεις
- TMB (tumor mutational burden) σε ειδικά σενάρια
- ειδικά χαρακτηριστικά όγκου/ιστολογίας και συνολική κλινική εικόνα
(Με λίγα λόγια: η ανοσοθεραπεία είναι “εξατομικευμένη” περισσότερο απ’ όσο φαίνεται.)
Τι να περιμένει ένας ασθενής από τη διαδικασία
Στις περισσότερες ενδείξεις, οι αναστολείς checkpoints δίνονται:
- ενδοφλέβια, σε τακτά χρονικά διαστήματα (π.χ. κάθε 2, 3, 4 ή 6 εβδομάδες ανά σχήμα),
- με παρακολούθηση αιματολογικών/βιοχημικών δεικτών,
- και απεικονιστικό επανέλεγχο σε προκαθορισμένα χρονικά σημεία.
Δεν είναι “ανώδυνη” θεραπεία, αλλά για αρκετούς ασθενείς είναι πιο ανεκτή από κλασικά σχήματα — πάντα όμως εξαρτάται από το φάρμακο και τον οργανισμό.
Παρενέργειες: διαφορετικές από της χημειοθεραπείας
Επειδή ενεργοποιείται το ανοσοποιητικό, μπορεί να εμφανιστούν ανοσο-σχετιζόμενες ανεπιθύμητες ενέργειες (immune-related adverse events), δηλαδή φλεγμονές σε όργανα, όπως:
- δέρμα (εξάνθημα/κνησμός)
- έντερο (διάρροια/κολίτιδα)
- ήπαρ (ηπατίτιδα με αύξηση τρανσαμινασών)
- πνεύμονας (πνευμονίτιδα)
- ενδοκρινείς αδένες (θυρεοειδίτιδα, επινεφριδιακή ανεπάρκεια κ.ά.)
Σημαντικό πρακτικό σημείο: πολλές από αυτές αντιμετωπίζονται (συχνά με κορτικοστεροειδή ή άλλους ανοσορυθμιστικούς παράγοντες), αλλά χρειάζονται έγκαιρη αναγνώριση.
Κόκκινες σημαίες που θέλουν άμεση επικοινωνία με την ομάδα σας:
- επιμονή ή επιδείνωση δύσπνοιας/βήχα,
- έντονη διάρροια ή αίμα στα κόπρανα,
- υψηλός πυρετός χωρίς προφανή αιτία,
- έντονη κόπωση με ζάλη/λιποθυμικά επεισόδια,
- έντονος πονοκέφαλος, διαταραχές όρασης ή σύγχυση.
Μύθοι και πραγματικότητα
- “Είναι φυσική θεραπεία;” Όχι. Είναι φαρμακευτική θεραπεία υψηλής τεχνολογίας, με αυστηρά πρωτόκολλα.
- “Δουλεύει σε όλους;” Όχι. Έχει εντυπωσιακά αποτελέσματα σε επιλεγμένες ομάδες, αλλά όχι καθολικά.
- “Αν δεν δουλέψει, δεν έχω άλλες επιλογές;” Συνήθως υπάρχουν εναλλακτικές: άλλα σχήματα, κλινικές μελέτες, συνδυασμοί ή διαφορετική στρατηγική ανάλογα με την κακοήθεια.
Ο ρόλος της ομάδας (και γιατί είναι “πολυπαραγοντική” απόφαση)
Η ανοσοθεραπεία δεν αποφασίζεται σε κενό. Στην πράξη, η καλύτερη επιλογή προκύπτει από:
- τύπο και στάδιο καρκίνου,
- μοριακό/παθολογοανατομικό προφίλ,
- προηγούμενες θεραπείες,
- συνοδά νοσήματα (π.χ. αυτοάνοσα),
- στόχους θεραπείας και ποιότητα ζωής.
Γι’ αυτό, η συζήτηση σε διεπιστημονικό ογκολογικό συμβούλιο (ογκολογικό board) έχει μεγάλη αξία.
Εφαρμογές της ανοσοθεραπείας ανά είδος κακοήθειας
Μελάνωμα
Η ανοσοθεραπεία αποτελεί βασικό πυλώνα θεραπείας, συχνά με αναστολείς PD-1 ως μονοθεραπεία ή με συνδυασμούς (π.χ. προσθήκη anti-CTLA-4 σε επιλεγμένους ασθενείς). Χρησιμοποιείται τόσο σε μεταστατική νόσο όσο και ως επικουρική/νεοεπικουρική θεραπεία σε συγκεκριμένα στάδια, με στόχο μείωση υποτροπής ή καλύτερο χειρουργικό έλεγχο.
Καρκίνος πνεύμονα (μη μικροκυτταρικός – NSCLC)
Εφαρμόζεται ευρέως, είτε ως μονοθεραπεία είτε σε συνδυασμό με χημειοθεραπεία, ανάλογα με βιοδείκτες (όπως PD-L1), ιστολογία και στάδιο. Σε ορισμένα πρωτόκολλα χρησιμοποιείται και πριν ή μετά από χειρουργείο/ακτινοθεραπεία σε επιλεγμένους ασθενείς.
Καρκίνος νεφρού (νεφροκυτταρικό καρκίνωμα)
Η ανοσοθεραπεία έχει σημαντικό ρόλο, συχνά με συνδυασμούς ανοσοθεραπείας μεταξύ τους ή ανοσοθεραπείας με στοχευμένη θεραπεία. Στόχος είναι καλύτερος έλεγχος της προχωρημένης/μεταστατικής νόσου και, σε επιλεγμένες περιπτώσεις, επικουρική θεραπεία μετά από νεφρεκτομή.
Ουροθηλιακός καρκίνος (ουροδόχος κύστη και ανώτερο ουροποιητικό)
Χρησιμοποιείται σε μεταστατική ή υποτροπιάζουσα νόσο, ιδιαίτερα όταν η χημειοθεραπεία δεν ενδείκνυται ή μετά από αποτυχία της. Σε επιλεγμένα πρωτόκολλα εφαρμόζεται και ως επικουρική θεραπεία μετά από ριζική επέμβαση, με στόχο τη μείωση κινδύνου υποτροπής.
Καρκίνοι κεφαλής και τραχήλου
Σε υποτροπή ή μεταστατική νόσο, η ανοσοθεραπεία (κυρίως anti-PD-1) μπορεί να αποτελέσει θεραπευτική επιλογή, είτε μόνη είτε σε συνδυασμούς, με βάση κλινικά χαρακτηριστικά και βιοδείκτες. Στόχος είναι παράταση ελέγχου της νόσου και διατήρηση ποιότητας ζωής σε κατάλληλους ασθενείς.
Ηπατοκυτταρικός καρκίνος (HCC)
Σε προχωρημένη νόσο, η ανοσοθεραπεία εφαρμόζεται σε συγκεκριμένα σχήματα, συχνά σε συνδυασμό με άλλους παράγοντες. Η επιλογή γίνεται με προσεκτική εκτίμηση ηπατικής λειτουργίας και συνολικής κατάστασης, καθώς η ασφάλεια/ανοχή είναι κρίσιμη.
Καρκίνοι οισοφάγου, γαστροοισοφαγικής συμβολής και στομάχου
Η ανοσοθεραπεία χρησιμοποιείται σε επιλεγμένες ενδείξεις, συχνά ως μέρος συνδυαστικών σχημάτων (π.χ. με χημειοθεραπεία) και ανάλογα με βιοδείκτες και στάδιο. Σε ορισμένες περιπτώσεις μπορεί να ενταχθεί επικουρικά ή σε μεταστατική νόσο, όταν υπάρχουν σαφή κριτήρια επιλογής.
Καρκίνος παχέος εντέρου και άλλοι γαστρεντερικοί όγκοι με MSI-H/dMMR
Ιδιαίτερη θέση έχει η ανοσοθεραπεία σε όγκους με υψηλή μικροδορυφορική αστάθεια ή έλλειμμα επιδιόρθωσης DNA (MSI-H/dMMR), όπου οι πιθανότητες ανταπόκρισης είναι μεγαλύτερες. Δεν αφορά όλους τους καρκίνους παχέος εντέρου, αλλά συγκεκριμένη βιολογική υποομάδα μετά από μοριακό έλεγχο.
Γυναικολογικές κακοήθειες (ενδομήτριο, τράχηλος)
Σε επιλεγμένες περιπτώσεις προχωρημένης ή υποτροπιάζουσας νόσου, η ανοσοθεραπεία μπορεί να χρησιμοποιηθεί, είτε μόνη είτε σε συνδυασμούς, συχνά με βάση βιοδείκτες και προηγηθείσες θεραπείες. Η εξατομίκευση είναι ιδιαίτερα σημαντική λόγω διαφορετικών βιολογικών υποτύπων.
Καρκίνος μαστού (τριπλά αρνητικός – TNBC)
Σε συγκεκριμένα κλινικά σενάρια, ιδιαίτερα όταν υπάρχουν οι κατάλληλες ενδείξεις/βιοδείκτες, η ανοσοθεραπεία εντάσσεται σε συνδυασμό με χημειοθεραπεία. Στόχος είναι η βελτίωση ανταπόκρισης και ελέγχου της νόσου σε επιλεγμένες ομάδες ασθενών.
Αιματολογικές κακοήθειες (λεμφώματα, λευχαιμίες, πολλαπλούν μυέλωμα)
Πέρα από τους αναστολείς checkpoints σε ορισμένους υποτύπους λεμφώματος, ιδιαίτερη σημασία έχουν οι κυτταρικές θεραπείες (CAR-T) και τα διειδικά αντισώματα, κυρίως σε υποτροπιάζουσες/ανθεκτικές μορφές. Πρόκειται για εξειδικευμένες θεραπείες με αυστηρή επιλογή ασθενών και στενή παρακολούθηση για ειδικές ανεπιθύμητες ενέργειες.
Με απλά λόγια (για όλους)
Η ανοσοθεραπεία είναι μια σύγχρονη θεραπεία του καρκίνου που βοηθά το ίδιο το ανοσοποιητικό μας να “δει” καλύτερα τα καρκινικά κύτταρα και να τα πολεμήσει. Δεν είναι κατάλληλη για κάθε τύπο καρκίνου ούτε για κάθε ασθενή, γι’ αυτό πριν αποφασιστεί συνήθως χρειάζονται ειδικές εξετάσεις στον όγκο (βιοδείκτες) και συζήτηση με την ογκολογική ομάδα. Σε ορισμένες κακοήθειες μπορεί να δώσει πολύ καλά και μερικές φορές μακροχρόνια αποτελέσματα, αλλά όπως κάθε θεραπεία μπορεί να έχει παρενέργειες — συχνά διαφορετικές από της χημειοθεραπείας — και γι’ αυτό χρειάζεται στενή παρακολούθηση και άμεση ενημέρωση του γιατρού αν εμφανιστούν νέα συμπτώματα.
Τελευταία ιατρική επιμέλεια: 27/01/2026 από τον Δρ. Γεώργιος Σάμπαλης, MD, PhD